Identifikasi Karbohidrat
Karbohidrat adalah polihidroksi aldehida atau keton dengan rumus empirik (CH2O)n, dapat diubah menjadi aldehida dan keton dengan cara hidrolisis, disusun oleh dua sampai delapan monosakarida yang dirujuk sebagai oligosakarida. Karbohidrat tersebar luas baik dalam jaringan hewan maupun jaringan tumbuh-tumbuhan. Dalam tumbuh-tumbuhan, karbohidrat dihasilkan oleh fotosintesis dan mencakup selulosa serta pati. Pada jaringan hewan, karbohidrat berbentuk glukosa dan glikogen. Fungsi karbohidrat yaitu, untuk sumber energi, pemanis pada makanan, penghemat protein, pengatur metabolisme lemak, penawar racun, baik untuk yang terkena konstipasi (sembelit), dan masih banyak lagi manfaat-manfaat yang lainnya.
Uji Anthrone
- Siapkan 12 buah tabung reaksi yang masih bersih dan telah di bilas dengan aquadest, serta di beri nomor 1 - 12, ke dalam masing - masing tabung reaksi di masukkan 2 ml pereaksi Anthrone
- Ke dalam tabung 1 di masukkan 0,2 ml aquadest (untuk blanko pereaksi) dan ke dalam tabung no 2 - 12 masing - masing di masukkan 0,2 ml larutan arabinosa 1%, fruktosa 1%, galaktosa 1%, glukosa 1%, laktosa 1%, maltosa 1%, sakarosa 1% amilum 1%, gom arab 1% (untuk kontrol positif) masing - masing larutan segera di campur dengan menggoyang - goyangkan tabung reaksi
- Perhatikan perubahan warna yang terjadi pada masing - masing tabung (hasil reaksi : terbentuk senyawa yang berwarna hijau atau biru kehijauaan)
Uji Seliwanoff
- Ke dalam 14 tabung reaksi yang bersih serta di beri nomor 1 - 14, ke dalam masing - masing tabung reaksi di masukkan 2,5 ml pereaksi Seliwanoff
- ke dalam tabung 1 di masukkan 5 tetes aquadest (untuk blanko pereaksi) dan ke dalam tabung no 2 - 3 masing - masing di masukkan 5 tetes fruktosa 1% dan sakarosa 1% (untuk kontrol positif)
- dan ke dalam tabung no 4 - 12 di masukkan 5 tetes larutan arabinosa 1%, galaktosa 1%, glukosa 1%, manosa 1%, laktosa 1% maltosa 1%,, maltosa 1%, maltosa 1%, dekstrin 1%, gom arab 1% (untuk kontrol negatif)
- masing - masing larutan di campur dengan cara menggoyang - gayangkan tabung reaksi
- dengan menggunakan penjepi tabung, masing - masing tabung di panaskan di atas pembakar bunsen secara hati - hati selama 20 detik atau dalam penangas air mendidih selama 1 menit
- di amati terbentuknya warna merah ceri pada masing - masing tabung
Uji Molisch
- Siapkan 12 buah tabung reaksi yang masih bersih dan telah di bilas dengan aquadest, serta di beri nomor 1 - 12, ke dalam masing - masing tabung reaksi 1 di masukkan 5 ml aquadest (untuk blanko pereaksi)
- Ke dalam tabung no 2 - 12 masing - masing di masukkan 5 ml larutan arabinosa 1%, fruktosa 1%, galaktosa 1%, glukosa 1%, laktosa 1%, maltosa 1%, sakarosa 1% amilum 1%, dekstrin 1%, gom arab 1% (untuk kontrol positif) masing - masing larutan segera di campur dengan menggoyang - goyangkan tabung reaksi
- Ke dalam masing - masing tabung di masukkan 2 tetes larutan pereaksi Molisch segar, larutan di campur dengan cara mengoyang - goyangkan tabung reaksi
- Ke dalam masing - masing tabung 1 -12, di masukkan 2,5 ml H2SO4 pekat secara perlahan - lahan melalui dinding tabung (hindari tabung tergoyang) . segera (sampai 5 menit setelah penambahan H2SO4 pekat) di amati terbentuknya cincin coklat pada bidang batas dua larutan dari masing - masing tabung
Uji Iodin
- siapkan 1 buah plat tetes 12 lubang yang bersih dan telah di bilas dengan aquadest serta di beri nomor 1 - 12 pada setiap lubang
- ke dalam tabung 1 di masukkan 1 tetes aquadest (untuk blanko pereaksi) dan ke dalam tabung 2 - 10 masing - masing di masukkan 1 tetes larutan arabinosa 1%, fruktosa 1%, galaktosa 1%, glukosa 1%, laktosa 1%, maltosa 1%, sakarosa 1%, gom arab 1% dan ke dalam tabung 11 - 12 masing - masing di masukkan satu tetes amilum 1%, dekstrin 1% (di gunakan sebagai kontrol positif) serta 1 tetes HCl 1N ke dalam masing - masing lubang
- ke 12 larutan di campur dengan menggunakan tusuk gigi (1 ujung tusuk gigi di pergunakan untuk satu lubang plat tetes) atau dengan cara mengoyang - goyangkan plat tetes
- ke dalam masing - masing larutan di atas di tambahkan 1 tetes larutan atau menggunakan tusuk gigi yang lain
- segera amati perubahan warna yang terjadi pada masing - masing lubang plat tetes (amilum berwarna merah coklat / merah anggur)
Uji Tollens
- ke dalam 12 buah tabung reaksi yang bersih dan telah di beri no 1 -12 masing - masing di masukkan 3 ml larutan AgNO3 0,1 N dan beberapa tetes larutan NH4OH 4N sampai endapan melarut kembali
- ke dalam tabung no 1 masukkan 3 ml aquadest (untuk blanko pereaksi) ke dalam tabung no 2 - 8 masing - masing di masukkan 3 ml larutan arabinosa 1%, fruktosa 1%, galaktosa 1%, glukosa 1%, manosa 1%, laktosa 1%, maltosa 1% (juga di gunakan untuk kontrol positif) dan dalam tabung reaksi no 9 - 12 masing - masing di masukkan 3 ml larutan sakarosa 1%, amilum 1% gom arab 1% (juga di gunakan sebagai kontrol negatif)
- masing - masing larutan di campur dengan cara menggoyang - goyangkan tabung reaksi . dengan menggunakan penjepit tabung, masing - masing tabung reaksi di panaskan di atas pembakar bunsen secara hati -hati
- di amati terbentuknya lapisan cermin pada masing - masing dinding tabung
Uji Osazon
- ke dalam 12 buah tabung reaksi yang bersih dan telah di beri no 1 -12 masing - masing di masukkan 2 ml larutan pereaksi Osazon
- ke dalam tabung no 1 masukkan 2 ml aquadest (untuk blanko pereaksi) ke dalam tabung no 2 - 8 masing - masing di masukkan 2 ml larutan arabinosa 1%, fruktosa 1%, galaktosa 1%, glukosa 1%, manosa 1%, laktosa 1%, maltosa 1% (juga di gunakan untuk kontrol positif) dan dalam tabung reaksi no 9 - 12 masing - masing di masukkan 2 ml larutan sakarosa 1%, amilum 1%, dekstrin 1%, gom arab 1% (juga di gunakan sebagai kontrol negatif)
- masing - masing tabung di tutup dengan aluminium foil dan di beri selotip, kemudian larutan di campur dengan cara menggoyang - goyangkan tabung reaksi . seluruh tabung di panaskan dalam penangas air mendidih selama 30 menit
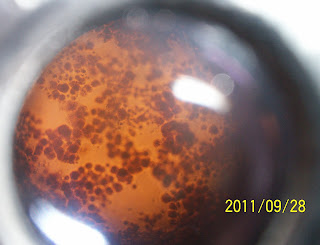
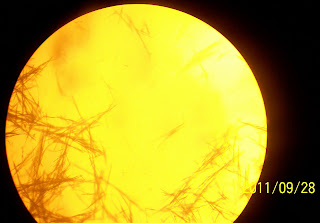
- dengan menggunakan pipet tetes bersih sedikit endapan / kristal di pindahkan ke kaca objek, lalu di amati dengan menggunakan mikroskop
- diamati perubahan warna yang terjadi pada masing - masing jenis monosakarida, setelah di amati secara mikroskopis










0 komentar:
Posting Komentar